吡哆醇依赖性癫痫(pyridoxine-dependent epilepsy, PDE)是一种罕见的常染色体隐性遗传病,在新生儿中会反复发作。PDE产生的原因是由于Aldh7a1基因突变导致赖氨酸代谢途径中的关键酶缺失,其有毒害性代谢物AASA/P6C累积。临床上发现体外补充高剂量的吡哆醇可以控制癫痫的发作,但有75%左右的患者仍然会存在智力障碍和/或发育迟缓的症状。鉴于吡哆醇治疗无法完全解决PDE患者的问题,深入探究Aldh7a1缺失在癫痫发作得到控制后如何损害大脑稳态的潜在机制迫在眉睫。
海马成体神经发生是哺乳动物大脑中一个独特的过程。在这个过程中,成体神经干细胞(neural stem cells, NSCs)可以通过增殖、分化和迁移一系列过程源源不断地产生新生神经元并整合到现有环路中。这一过程对维持大脑稳态和可塑性至关重要,并与学习、记忆及情绪调节等认知功能紧密相关。近期有研究表明,氨基酸及其代谢产物在成体神经发生的细胞代谢中发挥着关键作用,而氨基酸代谢的紊乱会严重损害成体神经发生和认知能力。基于此,探究赖氨酸及其代谢产物对海马成体神经发生的调控机制可能对PDE疾病如何损害大脑稳态提供思路。
本研究首先通过Aldh7a1f/f::Nestin-Cre小鼠构建了PDE小鼠模型,该小鼠模型能够表现临床病症特点。为了进一步探究ALDH7A1在成体神经发生中的作用,研究人员构建了Aldh7a1f/f::Nestin-CreERT2::Ai14 (Aldh7a1-iKO)小鼠模型。尽管Aldh7a1-iKO小鼠并未出现自发性癫痫发作,它们仍然在海马体依赖的认知测试中表现出明显的障碍。此外,该基因型小鼠表现出明显的海马成体神经发生异常,并且这种异常无法被高剂量的吡哆醇治疗所挽救。为了探究ALDH7A1介导的赖氨酸分解代谢调节神经发生的机制,该团队通过体外实验发现,只有在AASA/P6C处理下,NSCs才表现出与ALDH7A1缺陷的NSCs一致的增殖和分化上的缺陷。转录组分析进一步显示,在ALDH7A1缺陷的NSCs中,嘧啶代谢受到损害,而这种损害与吡哆醇的水平无关。此外,AASA/P6C给药还导致参与嘧啶从头合成的基因表达降低,而外源性嘧啶给药则可以治疗ALDH7A1缺陷小鼠的成体神经发生缺陷和认知障碍。
因此,ALDH7A1的缺失引起赖氨酸代谢中有毒代谢产物的积累,进而损害嘧啶的从头合成,从而抑制海马成体神经发生缺陷和认知能力受损,而嘧啶给药可以挽救成体神经发生缺陷和认知障碍。综上所述,该研究不仅阐明了癫痫患者存在智力障碍的潜在机制,而且为治疗癫痫患者的智力障碍提供了潜在的策略。
该研究于2024年4月发表在Science Advances杂志。中国科学院遗传与发育生物学研究所郭伟翔研究组闫健菲博士和吴俊杰博士为论文的共同第一作者,郭伟翔研究员为通讯作者。本研究得到国家重点研发计划、科技创新2030-“脑科学与类脑研究”和国家自然科学基金的支持。
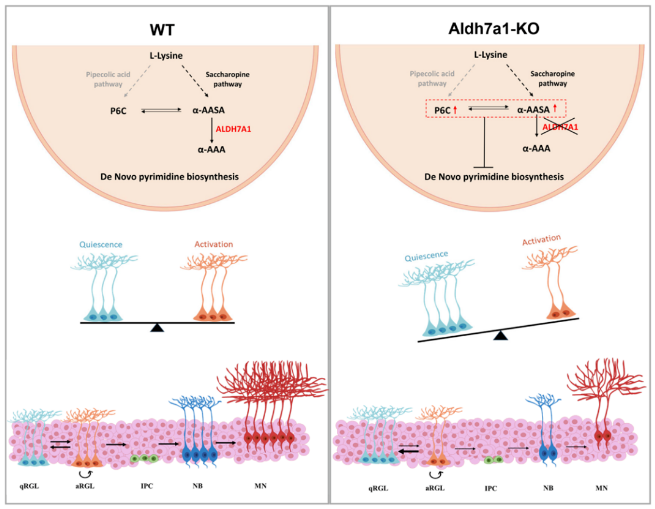
本研究发现简图(DOI:10.1126/sciadv.adl2764)
