代谢功能障碍相关脂肪性肝病(MASLD)是全球范围内最主要的肝脏代谢性疾病,患病率已超过三分之一。MASLD不仅会导致肝脏脂肪变性和炎症,还会显著增加慢性肾病、心血管疾病及糖尿病的风险。尽管已知肝脏铁负荷异常与脂质代谢紊乱是该病的重要特征,但如何通过精准调节脂质代谢网络来逆转病理进程,其背后的分子机制仍未被完全阐明。
2026年3月,中国科学院遗传与发育生物学研究所税光厚研究组在Free Radical Biology and Medicine杂志发表了题为Systemic lipid remodeling associated with deferoxamine treatment, dietary intervention and combinatorial effect in ameliorating high cholesterol diet-induced steatotic liver in mice的研究论文。该研究揭示了单唾液酸二己糖神经节苷脂(GM3)是调控MASLD脂质紊乱的核心分子,并提出铁螯合剂去铁胺(DFO)联合饮食干预是改善脂肪肝的全新策略。
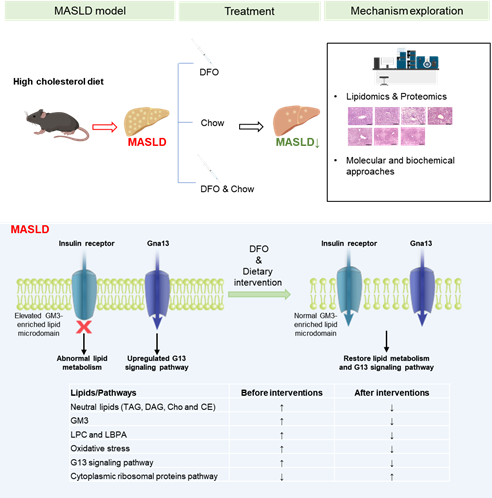
研究团队通过高胆固醇饮食(HCD)诱导的小鼠模型发现,肝脏中存在严重的脂质积聚和炎症反应。通过整合脂质组学与蛋白质组学技术,研究人员系统分析了不同干预手段下的代谢谱图。结果显示,DFO治疗能够显著降低肝脏铁含量并缓解炎症,而单纯的饮食干预则有效恢复胆固醇(Cho)和甘油三酯(TAG)的平衡。更为关键的是,研究发现GM3在病理状态下显著升高,而DFO与饮食干预的联合应用展现出强大的协同效应,能够共同下调质膜GM3水平,修复脂质与蛋白质的稳态平衡。
进一步的细胞实验证实了GM3在病理进程中的核心作用:通过沉默GM3合成酶降低GM3水平,可显著抑制肝细胞对胆固醇和脂肪酸的摄取,从而阻断脂质过量堆积。蛋白质组学富集分析表明,HCD诱导了SREBF和miR33调控的脂质合成通路以及氧化应激反应的异常激活,而联合干预能精准靶向并下调这些代谢通路,从分子层面逆转了代谢紊乱。
综上所述,该研究证实了饮食干预联合DFO治疗作为MASLD潜在干预策略的应用价值,而该小鼠模型的研究结果仍需在人体研究中进一步验证。
遗传发育所已毕业博士生倪震、王饶旭和苗唤为论文的共同第一作者,税光厚研究员为论文的通讯作者。该研究得到国家自然科学基金和中国科学院的项目资助
去铁胺联合饮食干预协同改善脂肪性肝病