髓鞘异常至今尚无有效治疗方法,是多种致残性神经系统疾病的根源,如多发性硬化症(MS)。虽然脂质占髓鞘的约70%,但对髓鞘形成至关重要的特定脂质,以及脂质代谢与髓鞘组装之间的机制,仍然不明确,阻碍了治疗开发。
2026年2月,中国科学院遗传与发育生物学研究所税光厚研究组在Journal of Translational Medicine杂志发表了题为Very long chain sphingolipids govern brain myelination by regulating oligodendrocyte differentiation and membrane microdomain integrity的研究论文。该研究定义了一种新型致病级联反应,即细胞自主丧失CerS2阻碍少突胶质细胞分化,超长链(VLC)鞘脂缺失破坏膜微域稳定,影响MBP定位,最终导致髓鞘化失败。这项工作将CerS2-VLC鞘脂轴定位为脱髓鞘疾病的潜在治疗靶点。
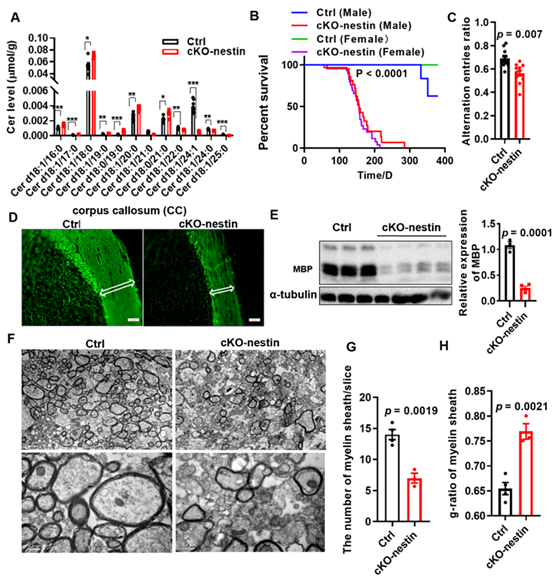
研究人员首先构建了中枢神经系统特异性(cKO-nestin)和少突胶质细胞特异性(cKO-OL)的神经酰胺合酶2(CerS2)条件性敲除小鼠。CerS2是合成C22–C24
超长链神经酰胺的关键酶。团队结合脂质组学、蛋白质组学和高分辨质谱成像(MSI)等多组学技术,系统描绘了CerS2敲除后脑内脂质和蛋白的异常变化,并通过行为学测试、电镜观察以及背根神经节(DRG)神经元-少突胶质细胞前体细胞(OPCs)体外共培养髓鞘形成实验,评估了相关的功能后果。结果显示,CerS2敲除小鼠表现出严重的神经表型,包括抽搐、早发性死亡以及显著的髓鞘形成不足。脂质组学揭示了一种病理性的脂质重塑:超长链鞘脂急剧减少,而短链(C16–C18)神经酰胺代偿性升高——这一脂质谱与多发性硬化症(MS)的临床特征高度相关。质谱成像证实,超长链鞘脂的缺失特异性地定位于受损的
白质纤维束区域。关键的挽救实验发现,野生型小鼠脑脂质提取物能够恢复CerS2敲除细胞的少突胶质细胞分化和体外髓鞘形成,而敲除小鼠自身的脑脂质提取物则无此效果。机制上,超长链鞘脂的缺失破坏了膜微区的完整性,导致髓鞘碱性蛋白(MBP)从脂筏中移位,从而阻碍正常髓鞘形成;而药物性破坏膜微区则可直接模拟出同样的髓鞘形成障碍。该研究结果不仅确立了 CerS2 缺陷与发育性髓鞘形成失败之间的因果关系,还为未来探究极长链鞘脂补充作为相关神经系统疾病治疗策略的研究奠定了重要基础。
遗传发育所已毕业博士生孙欢、博士生莫璐月和博士后曹明君为论文的共同第一作者,税光厚研究员和广州医科大学附属肿瘤医院的林茜雯教授为论文的共同通讯作者。该研究得到国家自然科学基金、国家重点研发计划和中国科学院的项目资助。
cKO-nestin小鼠的病理变化和髓鞘形成异常